Disfunkcija hepatalnog sistema uzrokovana primenom antituberkulotika
ANTITUBERCULOTIC-INDUCED LIVER DYSFUNCTION
SAŽETAK
Jetra je prva na udaru kod svih toksičnih oštećenja organizma zbog ogromne regenerativne sposobnosti svojih ćelija ona nije najviše oštećen organ lekovima. Osnovna patohistološka karakteristika oštećenja je hepatocelularna nekroza i masna infiltacija. Kao izraz reakcije preosetljivosti može se javiti holestaza.
Sagledavajući patoanatomske i laboratorijske nalaze kod oštećenja jetre antituberkuloticima može se reći da su izoniazid, rimfapicin i pirazinamod uslovno najviše hepatotoksični.
Studija je obuhvatila 215 pacijenata kod kojih je došlo do poremećaja funkcije jetre antituberkuloticima. Analizirani su biohemijski parametri oštećenja kao i kliničko ispoljavanje medikamentoznog hepatitisa.
Ključne reči: tuberkuloza, antituberkulotici, poremećaji funkcije jetre.
SUMMARY
The liver is the major target organ for any toxic events in an organism, but due to the impressive regenerative capacity of its cells, the liver is not the most drug-affected organ. The substential histopathological feature of the drug-induced liver damage is hepatocellular necrosis and fat infiltrations. The liver hypersensitivity reaction can be manifested as cholestasis. The study included 215 patients with manifested liver dysfunction induced by antituberculotic drugs. The analysis involved biochemical parameters and clinical symptoms of medicamentous hepatitis. Reviewing pathological anatomic and laboratoiry findings in antituberculotic-'induced liver dysfunction, isoniasid, rimphamycin and pirasinamod may be ranged among the most hepatotoxic antituberculotic drugs.
Key words: tuberculosis, antituberculotic drugs, liver dysfunctiuon
Mr sci med. Darinka Kukavica, Odeljenje za novootkrivenu tuberkulozu, Institut za plućne bolesti, Sremska Kamenica
UVOD
Jetra je prva na udaru kod svih toksičnih oštećenja organizma ali zbog ogromne regenerativne sposobnosti svojih ćelija ona nije najčešće oštećen organ toksičnim materijama. Do oštećenja jetre lekovima može doći u slučaju predoziranja, pokušaja suicida ali i kod normalne terapijske doze leka. (1,2)
Izoniazid patoanatomski izaziva steatozu i hepatitis dok je mehanizam dejstva dvojak a ispoljava se kao toksičnost i preosetljivost na lek, odnosno ima mešano dejstvo. Za pirazinamid je slična patogeneza oštećenja ali se patoanatomski češće nalazi hepatitis i holestaza. Rifampicin izaziva holestazu i hepatitis svim patogenetskim mehanizmima uključujući indukciju enzima citohrom P450. Istraživanja su pokazala da izoniazid i rifampicin zajedno izazivaju češće oštećenje jetre zbog kompeticije za isti enzimski sistem u mikrosomima. Zna se da izoniazid prolazi komplikovani metabolički put, delimično se pretvara u acetilizoniazid koji prelazi u izonikotinsku kiselinu i acetilhidrazin. Acetilhidrazin može biti metabolisan u toksični metabolit pomoću citohroma P450 koji indukuje rifampicin (3,4).
Laboratorijska dijagnostika pruža veliku pomoć ranim otkrivanjem povišenih transaminaza kao indeksa hepatocelularne nekroze, i to bez obzira da li dominira hepatitisni ili holestazni tip opštećenja jetre. Ovo uvećanje transaminaza promptno je vezano sa početkom bolesti za razliku od ekstrahepatične bilijarne opstrukcije kod koje se transaminaze povećavaju znatno kasnije. Za holestazni tip lekovima izazvanog hepatitisa karakteristično je i povišenje alkalne fosfataze udruženo sa porastom obe vrste bilirubina, konjugovanog i nekonjugovanog. Konjugovani bilirubin može se naći u mokraći ali se nalazi i urobilinogen zbog slobodne crevno-hepatične cirkulacije. Povećanje aktivnosti alkalne fosfataze kod hepatobilijarnih oboljenja je posledica povećane sinteze enzima u hepatocitima i epitelu žučnih kanalića, što je stimulisano od strane žučnih kiselina.
Povećana vrednost γ-GT događa se i u holestazi ali i u drugim hepatocelularnim oboljenjima, na primer alkoholna bolest jetre. Iako se smatra da je povećanje ovog enzima karakteristično za alkoholičare, ipak su vrednosti kod jedne trećine ovih osoba normalne. Ako su u holestazi povećani alkalna fosfataza i γ-GT, onda je sigurno da je alkalna fosfataza hepatobilijarnog porekla. Laboratorijska dijagnostika u toksičnim hepatitisima ipak nije u mogućnosti da razlikuje akutno toksični od akutnog virusnog hepatitisa (sem ako nije pozitivan HBs i HBeAg), ali je zato određivanje transaminaza i bilirubina u serumu od izvanrednog značaja za ocenjivanje stepena toksičnog uticaja na tkivo.
Klinička slika oštećenja jetre lekovima može biti različita. Prvi simptomi se pojavljuju u rasponu od druge do šeste nedelje. Oni mogu biti minimalni u smislu mučnine i lake nadutosti, pa sve do teških koji su praćeni žuticom i hepatičnom komom.
Kod oštećenja jetre izazvanog antituberkuloticima prvi neophodan terapijski korak je uklanjanje inkrimisanog leka, često se time zaustavlja dalje oštećenje jetre. Lečenje kortikosteroidima pokušavano je ukoliko bolest nastavlja svoj klinički tok, ali rezultati nisu ubedljivi. Ukoliko preovađuje oštećenje jetre toksičnog tipa sa masivnom hepatocelularnom nekrozom, terapija kortikosteroidima definitivno nema uspeha. Upotreba sredstava za rehidraciju, hepatoprotektiva i simptomatika ublažava simptome i omogućava bržu regeneraciju hepatocita. Specifičnog antidota nema. Pri ponovnom uvođenju lekova treba biti obazriv, pomno pratiti kliničke simptome bolesti a laboratorijske nalaze češće kontrolisati.
MATERIJAL I METODE
Studija je otpočeta 1998. godine i obuhvatila u kontinuitetu 215 bolesnika kod kojih je dokazana tuberkuloza plućne ili vanplućne lokalizacije. Analizirani su biohemijski parametri funkcije jetre na dolasku, a potom svakih sedam dana nakon uvođenja antituberkulotika: bilirubini (direktni i ukupni), transaminaze (aspartat, aminotransferaza - AST i alanin aminotransferaza - ALT), alkalna fosfataza - AP, laktat dehidrogenaza - LDH, gama glutamin transpeptidaza ili transferaza - γ -GT, proteinogram i HbSAg.
Biohemijski parameri su rađeni u Zavodu za biohemiju Instituta. Rezultati su prezentovani u radu tekstualno, tabelarno i grafički.
REZULTATI ISTRAŽIVANJA
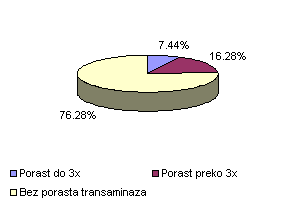
Porast transaminaza
Na uzorku od 215 pacijenata porast transaminaza do 3 puta imalo je 16 pacijenata (7,44%) a porast preko 3 puta imalo je 35 pacijenata (16,28%). Porast transaminaza preko 3 puta bio je uslov za prekidanje terapije. Transaminaze nisu rasle kod 164 bolesnika (76,28%).
|
|
Broj pacijenata |
% |
|
Porast do 3x |
16 |
7,44 |
|
Porast preko 3x |
35 |
16,28 |
|
Bez porasta transaminaza |
164 |
76,28 |
|
Ukupno |
215 |
100,00 |
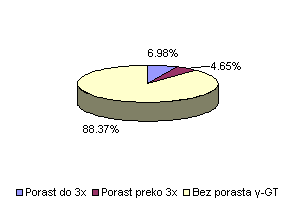
Porast γ-GT
Na uzorku od 215 pacijenata porast γ-GT do 3 puta iznad norme imalo je 15 pacijenata (6,98%) a porast preko 3 puta imalo je 10 pacijenata (4,65%). Ovaj enzim nije rastao kod 190 bolesnika (88,37%).
|
|
Broj pacijenata |
% |
|
Porast do 3x |
15 |
6,98 |
|
Porast preko 3x |
10 |
4,65 |
|
Bez porasta γ-GT |
190 |
88,37 |
|
Ukupno |
215 |
100,00 |
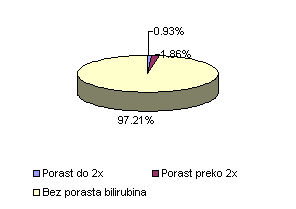
Porast bilirubina
Na uzorku od 215 pacijenata 2 pacijenta su imala porast bilirubina do 2 puta iznad norme (0,93%) i 4 pacijenta su imala porast preko 2 puta (1,86%). Porast bilirubina preko 2 puta bio je jedan od uslova za skidanje terapije. Bilirubini nisu rasli kod 209 bolesnika (97,21%).
|
|
Broj pacijenata |
% |
|
Porast do 2x |
2 |
0,93 |
|
Porast preko 2x |
4 |
1,86 |
|
Bez porasta bilirubina |
209 |
97,21 |
|
Ukupno |
215 |
100,00 |
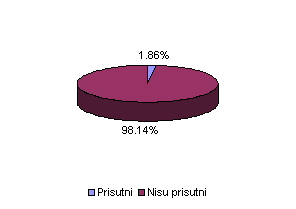
Klinički znaci medikamentoznog hepatitisa
Od 215 pacijenata 211 nije imalo kliničke znake medikamentoznog hepatitisa (98,14%). 4 pacijenta su imala kliničke znake medikamentoznog hepatitisa (1,86%), pri čemu je 1 bolesnik imao jasno izraženu žuticu.
|
|
Broj pacijenata |
% |
|
Prisutni |
4 |
1,86 |
|
Nisu prisutni |
211 |
98,14 |
|
Ukupno |
215 |
100,00 |
Biohemijske analize imaju veliki značaj u dijagnostici oboljenja jetre. Zajedno sa kliničkim podacima one omogućavaju otkrivanje oboljenja, utvrđivanje njegove prirode, težine, toka i prognoze. Testovi integriteta hepatocita uključuju merenje transaminaza (AST i ALT), dehidrogenaza (najčešće laktat i glutamat) i drugih enzima u serumu. Visina porasta enzima zavisi od stepena oštećenja ćelijskog integriteta koje se kreće od povećanog permabiliteta membrane do ćelijske nekroze. U hepatologiji se najčešće određuju vrednosti transaminaza, te je njihova povećana aktivnost vrlo osetljiv pokazatelj oštećenja hepatocita. Obe transaminaze se nalaze u skeletnim i srčanom mišiću kao i u bubrezima. Međutim, aktivnost ALT je najveća u hepatocitima te se može smatrati specifičnim parametrom hepatocelularnog oštećenja. Odnos ALT/AST (De-Ritisov količnik) je normalno manji od 1,0, a kod oštećenja jetre raste, jer više (i do 1.000 puta) raste ALT koja je smeštena pretežno u citosolu hepatocita. Obrnut odnos transaminaza i izraženiji porast AST događa se kod težih i dubljih oštećenja hepatocita kada se oslobađaju enzimi iz mitohondrija. U fulminantnom hepatitisu pad aktivnosti ovih enzima nagoveštava terminalni stadijum zbog iscrpljenosti enzimske sinteze.
Biohemijske metode određivanja poremećaja bilijarne ekskrecije - holestaze podrazumevaju merenje bilirubina, njegovih metabolita i aktivnosti enzima holestaze čije oslobađanje zavisi od stepena holestaze. Kvantitativno određivanje bilirubina u serumu je jedan od najstarijih testova za ispitivanje funkcije jetre. Konjugovani bilirubin je rastvorljiv u vodi i direktno reaguje sa dijazo reagensom. Konjugovane hiperbilirubinemije sa povišenim pretežno direktnim bilirubinom u serumu ukazuju na postojanje poremećaja žuči na nivou hepatocita (hepatocelularni ikterus) ili žučnih puteva (opstruktivni ikterus). Nekonjugovane hiperbilirubinemije nastaju zbog poremećaja konjugacije bilirubina pri čemu se nivo ukupnog bilirubina penje iznad norme. Zbog velikog kapaciteta jetre ovi parametri su sami za sebe nisko senzitivni u prepoznavanju vrste i težine oboljenja i zbog toga nemaju veliki prognostički značaj.
Određivanje enzima holestaze kao što su alkalna fosfotaza (AP) i gama-glutamil transpeptidaza (γGT) su parametri koji pomažu u daljem diferenciranju žutica. Oni se oslobađaju sa biomembrane hepatocita i povećano sintetišu i toku holestaze. Lako povećanje AP (jedan do dva puta) viđa se kod mnogih parenhimskih oboljenja jetre a kod ozbiljnih medikamentoznih hepatitisa vrednosti mogu rasti i do deset puta. Međutim, povećana aktivnost AP u serumu nije specifična samo za oboljenja jetre i sreće se u nizu drugih stanja i oboljenja (hiperparatireoidizam, metastaze u kostima, karcinom bronha). Samim tim nije moguće proceniti težinu i prognozu hepatobilijarnog oboljenja. Povećane vrednosti γGT se sreću već kod malog poremećaja integriteta hepatocita ili male holestaze, naročito kod alkoholičara. Uprkos velikoj osetljivosti ovog enzima mala specifičnost ograničava njegovu širu primenu u kliničkoj praksi.
U našoj studiji na ukupnom broju ispitanika su analizirane vrednosti transaminaza< bilirubina, γGT, kao i bolesnici sa kliničkim znacima medikanentoznog hepatitisa. Na uzorku od 215 ispitanika koji su praćeni u vremenskom kontinuitetu od dve godine porast transaminaza do tri puta iznad norme imalo je 16 ispitanika, odnosno 7,44%, a preko tri puta 35 odnosno 16,28% obolelih. Samo je 4,65% ispitanika imalo trostruki porast γGT a 1,86% obolelih porast bilirubina preko dva puta. Analizirajući studije rađene u svetu, pokazalo se da su naši rezultati u saglasnosti sa većinom od njih. U velikoj studiji nemačkih autora Schaberga i saradnika koja je obuhvatala 519, bolesnika oštećenje jetre sa porastom transaminaza nađeno je kod 11% ispitanika. Faktički, oko polovine nuzefekata antituberkulotika u ovoj studiji pripada medikamentoznom oštećenju jetre (5,2). Jedanaestogodišnja kontrolisana studija rađena u Danskoj pokazuje ralativno nizak nivo hepatotoksičnosti antituberkulotika (oko 8%) kod pacijenata (6). S druge strane, autori iz Indije Sigh, Garg, Tandora visok procenat medikamentoznog oštećenja jetre u njihovoj populaciji objašnjavaju još jednim faktorom rizika, a to je malnutricija (3,7,8).
Klinička slika medikamentoznog hepatitisa u našoj studiji razvila se kod malog broja neselektiranih bolesnika, svega četiri ili 1,86%. To se može objasniti dobrim monitorisanjem funkcije jetre i relativno ranim prekidom terapije (kriterijum za ukidanje lekova je bio trostruki porast transaminaze iznad norme), pri čemu se nije čekao razvoj kliničkih znakova medikamentoznog hepatitisa. Slični procenti se prate i u radovima drugih autora. Tomson beleži 3% dijagnostikovanih sa kliničkim znacima medikamentoznog hepatitisa (9-13).
Važnost ranog prepoznavanja toksičnog oštećenja jetre je sprečavanje fulminantnog hepatitisa i smrti. Objektivno govoreći, nuzefekti lekova često rezultiraju modifikaciju ili diskontinuiranu terapiju. Kod ambulantnih bolesnika neophodna je hospitalizacija (13-18).
ZAKLJUČCI:
Naša studija je pokazala da:
- Antituberkulotici prve linije dovode do oštećenja funkcije jetre u 16,28% slučajeva, međutim klinički znaci medikamentoznog hepatitisa se javljaju kod svega 1,86% bolesnika.
- Antituberkulotike ne treba ukidati pre petostrukog porasta transaminaza iznad normalnih vrednosti ukoliko se ne pojave klinički znaci medikamentoznog hepatitisa.
- Dovoljne biohemijske analize u rutinskom praćenju mogućih toksičnih oštećenja jetre antituberkuloticima jesu određivanje bilirubina i transaminaza u serumu, uz kliničko praćenje bolesnika.
LITERATURA
- Goldman AL, Braman SS. Isoniazid: a review with emphasis on adverse effects. Chest 1972; 62: 71-77.
- Schaberg T, Rebhan K, Lode H. Risk factors for side-effects of isoniazid, rifampin and pyrazinamide in patients hospitalized for pulmonary tuberculosis. Eur Respir J. 1996; 9(10): 2026-30.
- Singh J, Garg PK, Tandon RK. Hepatotoxicity due to antituberculosis therapy. Clinical profile and reintroduction of therapy. J Clin Gastroenterol. 1996 Apr; 22(3): 211-14.
- Altman C, Biour M, Grange JD. epatic toxicity of antitubercular agents. Role of different drugs. 199 cases. Presse Med. 1993 Sep 11; 22(26): 1212-16.
- Stanulović M. Antituberkulotici U: Farmakoterapija u pulmologiji. Varagić V, Stevanović M. Ed Elit-Medica, Beograd, 1998; 154-65.
- Dossing M, Vilcke JT, Askogard DS, Nybo B.Liver injury during antituberculosis treatment: an 11- year study, Tuber Lung Dis 1996; 77 (4); 335-40.
- Grosset J, Leventis S.Adverse effects of rifampin, Rev Infect Dis 1983; 5(Suppl 3): 5440-6.
- Chan CH, Or KK, Cheung W, Woo J.Adverse drug reaction and outcome of elderly patients of antituberculosis chemotherapy with and without rifampicin. J Med 1995; 26 (1-2): 43-52.
- Thompson NP, Ceplin ME, Hamilton MI et al: Antituberculosis medication and the liver: dangers and recommendations in management, Eur Resp J 1995; 8 (8): 1384-8.
- Farrell FJ, Keeffe EB, Man KM, et al.Treatment of hepatic failure secondary to isoniazid hepatitis with liver transplantation. Dig Dis Sci 1994 Oct; 39(10):2255-9.
- Teleman MD, Che CB, Ernest A et al.Hepatotoxycity of tuberculosis chemotherapy under geueral programme condition Singapore, Int J Tuber Lung Dis 2002; 6 (8): 699-705.
- Devato FM, Gonzalez C, Jannantuono R. et al: Risk factors for hepatotoxcity induced by antituberculosis drugs, Acta Physiol Pharmacol Their Latinoam 1997; 47 (4): 197-202.
- Pande JN, Sigh SP, Khilnani GC et al. isk factors for hepatotoxicity from antituberculosis drug a case sontrol study, Thorax 1996; 51 (2): 132-6.
- Yee D, Valiquette C, Pelletter M et al.Incidence of serious side effects from first line antituberculosis drugs among patiens treated for active tuberculosis., Am J Resp Crit Care Med 2003; 167 (11) 1472-7.
- Durand F, Jerbrak G, Pessayre D et al. epatotoxicity of antitubercular treatments. Rationale for monitoring live status. Durg - Saf 1996; 15 (6): 394-405.
- Lee AM, Mennorie JZ, Jones RC et al.Risk factors for hepatotoxiciti associated vith rifampin and pyrazinamide for the treatment of latent tuberculosis infect expirience from three public health tuberculosis clinics, Int J Tuberc Lung Dis 2002; 6 (11): 995-1000.
- Mc Neill L, Allen M, Estrada C et al.Pyrazinamide and rifampin us isoniazid for the treatment of latent tubersulosis improved complection rates but more hepatotoxicity, Chest 2003; 123 (1): 102-6.
- Charles M, Nolan MD, Stefan V. et al.Hepatotoxicity associated vith isoniazid preventive therapy, JAMA 1999; 281: 1014-8.